Перейти к:
Определение режимов безопасного применения селективной микроимпульсной индивидуальной ретинальной терапии макулярной зоны с помощью моделирования на основе теории активированного комплекса
https://doi.org/10.37895/2071-8004-2023-27-2-22-31
Аннотация
Цель: провести моделирование различных режимов лазерного излучения, оценить степень повреждения ретинального пигментного эпителия и прилежащих структур и определить режимы и условия безопасности селективной микроимпульсной индивидуальной ретинальной терапии на основе теории активированного комплекса.
Материалы и методы. Моделирование степени повреждения хориоретинального комплекса и прилежащих структур проводили на основе теории активированного комплекса с помощью уравнения Эйринга. Для определения качества режима и условий безопасности применяли следующие определения. Микроимпульсный режим – режим с фиксированными значениями длительности микроимпульса, рабочего цикла и количеством импульсов в пакете, мощность – изменяемый параметр. Эффективность – отношение количества денатурированного белка внутри слоя ретинального пигментного эпителия к общему количеству белка в нем. Селективность – отношение количества денатурированного белка внутри слоя ретинального пигментного эпителия к общему количеству денатурированного белка. Относительная вредность – отношение объема денатурированного белка за пределами ретинального пигментного эпителия к объему белка в нем.
Результаты и обсуждение. Определено качество микроимпульсного режима в зависимости от значения селективности при эффективности, равной 90 %. При значении эффективности менее 50 % режим является неселективным, более 67 % – селективным. Установлены условия безопасности применения селективных микроимпульсных режимов с учетом сохранности нейросенсорной сетчатки и хориоидеи по показателю относительной вредности, который не должен превышать единицы. Определены параметры, при которых микроимпульсные режимы обладают высокими значениями (более 90–99) эффективности и селективности одновременно. Для этого требуется режим единичного импульса, длительность микроимпульса от 25 мкс и мощность от 6 до 8 Вт. Для расширения комбинации параметров необходима возможность их свободного изменения с шагом в 1 импульс, 5 мкс, 100 мВт, с продолжительным интервалом и коротким рабочим циклом. Эти технические возможности могут быть реализованы и внедрены в клиническую практику производителями лазерных аппаратов.
Заключение. Для селективной микроимпульсной индивидуальной ретинальной терапии макулярной зоны на существующих лазерах могут применяться микроимпульсные режимы с длительностью импульса не более 200 мкс, коротким рабочим циклом менее 5 % и количеством импульсов в пакете не более 5, относительной вредностью менее единицы, с подбором мощности излучения, учитывающей персональные особенности пациента.
Ключевые слова
Для цитирования:
Иванова Е.В., Володин П.Л. Определение режимов безопасного применения селективной микроимпульсной индивидуальной ретинальной терапии макулярной зоны с помощью моделирования на основе теории активированного комплекса. Лазерная медицина. 2023;27(2):22-31. https://doi.org/10.37895/2071-8004-2023-27-2-22-31
For citation:
Ivanova E.V., Volodin P.L. Determination of modes for safe application of selective micro-pulse individual retinal therapy of the macular zone using the modeling based on the theory of activated complex. Laser Medicine. 2023;27(2):22-31. (In Russ.) https://doi.org/10.37895/2071-8004-2023-27-2-22-31
Памяти Георгия Ивановича Желтова посвящается
«Углубление знаний о процессах воздействия нефизиологичного (не имеющего аналогов в природе) лазерного излучения на ткани и органы человека последовательно выявляет новые факторы риска; эти факторы указывают на необходимость постоянной корректировки как сложившихся представлений, так и адекватного повышения жесткости действующих норм лазерной безопасности, то есть снижения предельно допустимых уровней облучения людей».
Г.И. Желтов (2013)
ВВЕДЕНИЕ
В настоящее время в офтальмологии применяются лазерные приборы с широким диапазоном параметров, улучшенной оптикой, визуализацией, фокусировкой и доставкой излучения, что открывает новые возможности в лечении заболеваний макулярной области, включая фовеальную аваскулярную зону сетчатки [1]. Лазерное лечение в фовеа, которая ответственна за максимальные зрительные функции, должно происходить с сохранением структурного и функционального состояния нейросенсорной сетчатки и хориоидеи. Данный подход на серийных лазерных установках реализуется при технологии селективной микроимпульсной индивидуальной ретинальной терапии (СМИРТ) [2]. Основными проблемами применения селективных микроимпульсных режимов в клинической практике являются отсутствие визуального контроля, сложность подбора параметров и необходимость поиска баланса между достижением клинического результата и возможным ятрогенным эффектом.
Селективное воздействие не определяется офтальмоскопически, но приводит к дозированному повреждению ретинального пигментного эпителия (РПЭ), которое регистрируется по данным аутофлуоресценции (АФ) [2]. Участки в области нанесения лазерных аппликатов визуализируются как гипофлуоресцентные пятна [3][4]. Повреждение нейросенсорной сетчатки и хориоидеи не регистрируется современными методами диагностики, однако определяется с помощью компьютерного моделирования [5]. Корректно построенная модель может предсказать повреждение РПЭ по данным АФ и уровень термоденатурации прилежащих тканей [6][7].
На серийных лазерных установках с микроимпульсным режимом, предназначенных для лечения заболеваний глазного дна, основной механизм повреждения хориоретинального комплекса (ХРК) происходит за счет термоденатурации протеинов [8][9]. В офтальмологии для моделирования процессов повреждения РПЭ и прилежащих структур используются физические модели на основе интеграла Аррениуса [7][10][11]. Показатели А и ΔЕ из уравнения Аррениуса не являются термодинамическими величинами, их значения зависят от условий проведения эксперимента и фитируются (подбираются) для лучшего соответствия наблюдаемым данным. В работах по изучению воздействия лазерного излучения на ткани глаза наблюдается разброс энергии активации для белков ХРК в широком диапазоне [10][12]. Термодинамическая стабильность соединений белков и, как следствие, процессы необратимой тепловой денатурации практически не зависят от генетического многообразия популяции [13][14]. Следовательно, значения энергии активации для белков ХРК одного и того же вида не могут сильно отличаться. Поэтому более корректно проводить моделирование на основе теории активированного комплекса (ТАК), в которой используются классические термодинамические показатели для белков. Энтропия и энтальпия (свободная энергия Гиббса) белкового комплекса определяются по стандартизированной методологии на основании калориметрических измерений с высокой точностью. Модель на основе ТАК не требует подбора термодинамических параметров и предпочтительна для оценки повреждения ХРК человека. Результаты модели на основе ТАК с показателями ΔH и ΔS для комплекса белков и других органических структур РПЭ, определенных Г. И. Желтовым и соавт., совпадают с результатами тестирования микроимпульсного режима по данным коротковолновой АФ [6].
Определение с помощью полученной модели уровня необратимой термоденатурации нейросенсорной сетчатки и хориоидеи позволяет рассчитать безопасные режимы для СМИРТ, ввести новые требования к безопасности применения лазерного излучения, которые кроме облученности и формирования очага коагуляции учитывают более деликатные повреждения ХРК.
Цель исследования: провести моделирование различных режимов лазерного излучения, оценить степень повреждения ретинального пигментного эпителия и прилежащих структур и определить режимы и условия безопасности селективной микроимпульсной индивидуальной ретинальной терапии на основе теории активированного комплекса.
МАТЕРИАЛЫ И МЕТОДЫ
Подробное описание компьютерной модели по воздействию лазерного излучения на ХРК глаза, совпадающей с результатами тестирования микроимпульсного режима по данным АФ, представлено в совместной работе с доктором физико-математических наук А. В. Гуськовым [7]. Параметры физической модели: длина волны – 577 нм, плоская форма пучка, диаметр пятна – 100 мкм, коэффициент пропускания – 37 %, поглощение нейроэпителием – 13 %, коэффициент поглощения РПЭ – 460 см-1, толщина слоя РПЭ – 10 мкм. Компьютерная модель на основе ТАК с уравнением Эйринга и показателями ΔH и ΔS для комплекса органических структур и белков РПЭ, определенных in vivo в серии лазерных экспериментов на животных Г. И. Желтовым и соавт. [15][16], предсказывающая повреждение РПЭ по данным АФ, представлена в предыдущей статье [6]. Графики были построены с использованием программ «ROOT» и Microsoft Office Excel.
Определение и характеристики микроимпульсного режима следующие. Микроимпульсный режим – режим с фиксированными значениями длительности микроимпульса, рабочего цикла и количеством импульсов в пакете (длина волны – 577 нм, диаметр пятна – 100 мкм), мощность является изменяемым параметром.
Для количественной оценки избирательности и степени повреждения РПЭ и прилежащих структур были введены следующие понятия. Эффективность – отношение количества денатурированного белка внутри слоя РПЭ к общему количеству белка в РПЭ. Селективность – отношение количества денатурированного белка внутри слоя РПЭ к общему количеству денатурированного белка. Степень сохранности нейросенсорной сетчатки определяется объемом повреждения тканей, прилежащих к РПЭ. Вредность отражает повреждение нейросенсорной сетчатки и хориоидеи и характеризует абсолютный «вред», наносимый лазерным воздействием, без учета РПЭ. Относительная вредность равна отношению объема денатурированного белка за пределами РПЭ к объему белка в РПЭ, или равна отношению значения вредности к объему РПЭ (рис. 1).
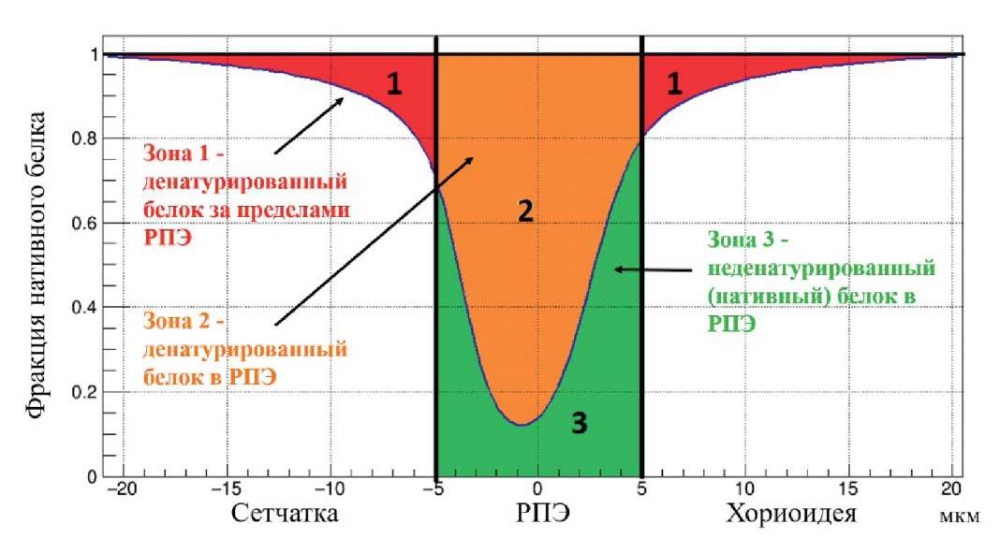
Рис. 1. Пример распределения фракции нативного
и денатурированного белка в центре пятна воздействия
Fig. 1. Example of the distribution of native
and denatured protein fraction at the center of irradiated spot
РЕЗУЛЬТАТЫ И ОБСУЖДЕНИЕ
1. Моделирование единичного импульса
Рассмотрим профиль температуры и область распределения нативного и денатурированного белка на примере единичного импульса длительностью 80 мкс и мощностью 2,0 Вт. Компьютерное моделирование проводили при условии, что в РПЭ абсорбируется 37 % лазерного излучения с коэффициентом поглощения 460 см-1. Как видно на рисунке 2, при моделировании единичного импульса для конкретного человека с фиксированными показателями пропускания и поглощения, практически вся зона повреждения локализована в области РПЭ. Значения эффективности, селективности и вредности составляют 70, 97 и 0,1 соответственно.
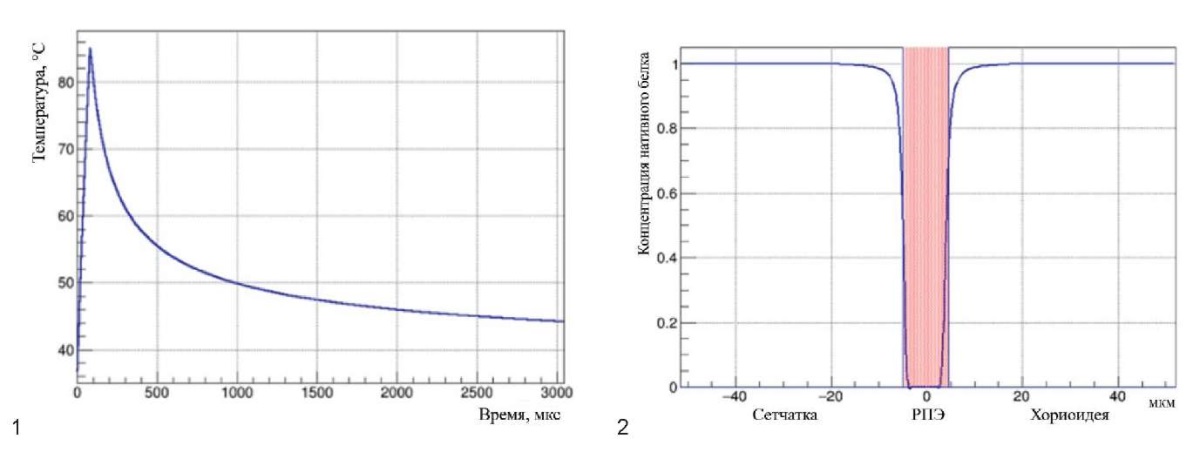
Рис. 2. Моделирование единичного импульса
длительностью 80 мкс и мощностью 2,0 Вт (100 мкм, 577 нм).
1 – распределение температуры в центре пятна воздействия;
2 – фракции нативного и денатурированного белка
в центре пятна воздействия
Fig. 2. Modeling of a single pulse
with duration 80 ms and power 2.0 W (100 microns, 577 nm).
1 – distribution of temperature in the center of targeted spot;
2 – fractions of native and denatured protein at the center of irradiated spot
2. Построение кривых эффективности и селективности
Меняя значения мощности при компьютерном моделировании, получим кривые эффективности и селективности в зависимости от мощности для конкретного режима в диапазоне от 0 до 100 %. На рисунке 3 на примере единичного импульса длительностью 50 мкс представлены зависимости эффективности и селективности от мощности. Как видно, с ростом мощности эффективность увеличивается, а селективность падает. Диапазон мощности можно разделить на три зоны. При значениях мощности до 2,5 Вт значения селективности высокие, а эффективности – низкие. Таких параметров будет недостаточно для достижения клинического результата. При мощности выше 4 Вт показатели эффективности высокие, а селективности – наоборот, низкие. Применение таких параметров приведет к повреждению нейросенсорной сетчатки и хориоидеи. В диапазоне мощности от 2,5 до 4,0 Вт значения эффективности и селективности являются высокими одновременно, что оптимально для клинического применения.
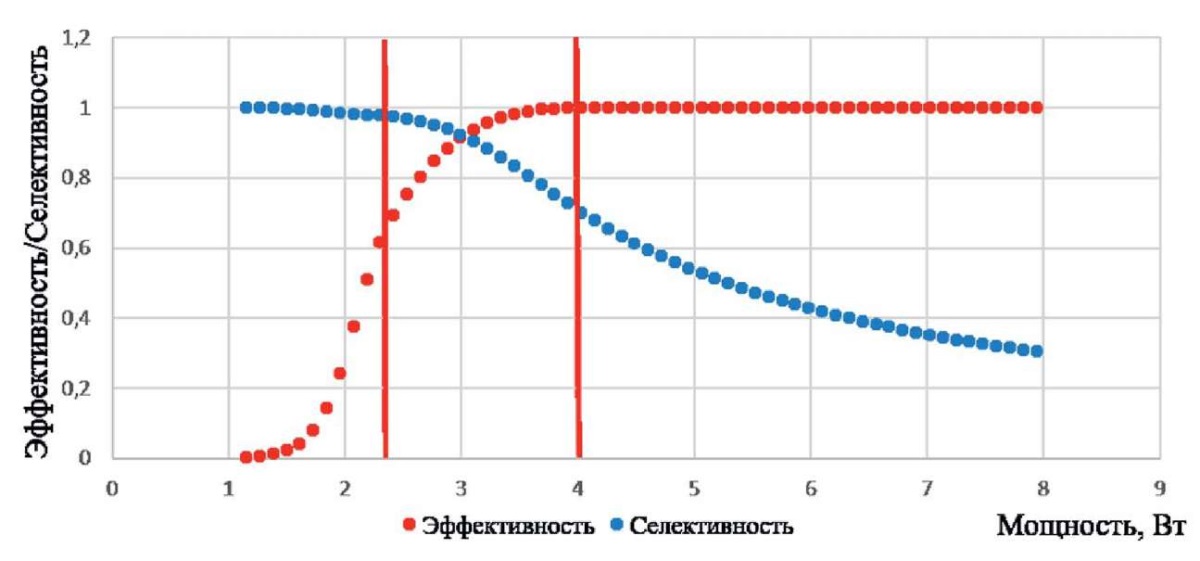
Рис. 3. Зависимость эффективности и селективности от мощности
для микроимпульсного режима единичного импульса длительностью 50 мкс
Fig. 3. Dependence of efficiency and selectivity on the power
for single pulse micropulse mode with duration 50 µs
Обычно в литературе уровень повреждения описывается омегой (Ω), а порогом считается значение омега (Ω) = 1 [10]. Связь эффективности и омеги (Ω) описывается уравнениями 1 и 2.
Ω = ln(1/1 – Эффективность)) (1)
Эффективность = 1 – e–Ω (2)
Однако для получения достоверного клинического результата значение эффективности должно быть 90 % [2]. Поэтому чтобы охарактеризовать качество эффективного лазерного воздействия, введем порог η = 90 и ζ (η = 90) – это значение селективности режима при эффективности, равной 90 %. Таким образом, определим три порога качества режима в зависимости от значений селективности при фиксированном значении эффективности 90 %: 1 – неселективный режим: ζ (η = 90) < 50 %; 2 – умеренно селективный режим: 50 % < ζ (η = 90) < 67 %; 3 – селективный режим: ζ (η = 90) > 67 %.
3. Эффективно-селективные кривые
Если на основе графиков из рисунка 3 построить зависимость селективности от эффективности, то получится эффективно-селективная кривая для конкретного режима (рис. 4). Эффективно-селективная зависимость, по данным компьютерного моделирования, является инвариантной по отношению к изменению персональных свойств пациентов, то есть может быть рассчитана для любого человека и будет верна для всех других. Это означает, что если для конкретного пациента подобрать необходимую мощность для достижения необходимой эффективности, то уровень селективности для данного режима будет определяться на основе данной кривой для любого пациента. При отсутствии эффективно-селективной области для данного режима достичь ее только изменением мощности невозможно и потребуется поменять параметры самого режима. Например, как видно, режим 50 мкс, 2,4 %, 20 мс (10 импульсов) ни при каких условиях не попадает в окно с высокой селективностью. С увеличением эффективности за счет подъема мощности происходит снижение селективности. Улучшение селективности с требуемой эффективностью возможно только за счет изменения самого режима, например уменьшения количества импульсов.
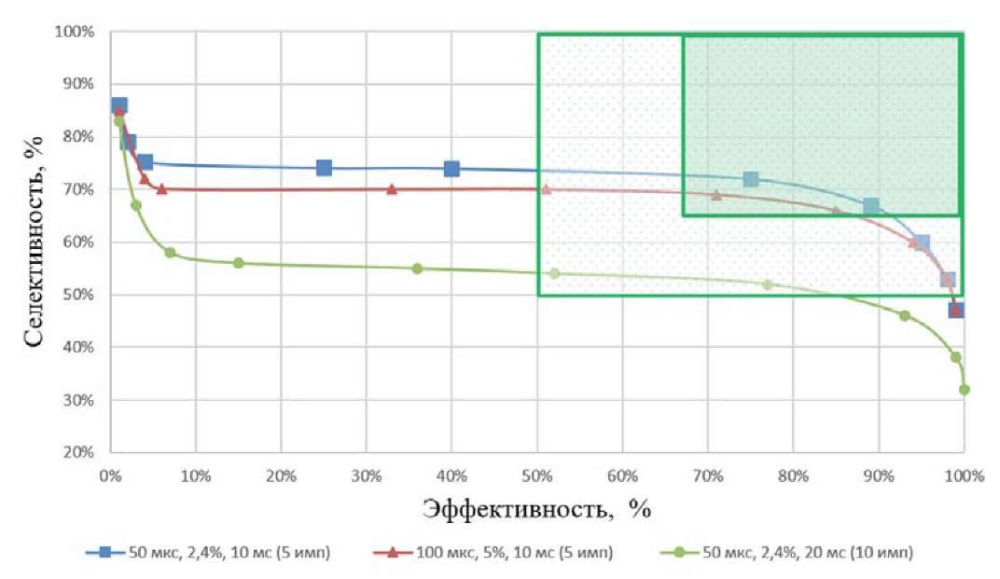
Рис. 4. Зависимость селективности от эффективности
для различных микроимпульсных режимов
Fig. 4. Dependence of selectivity on the efficiency
for various micropulse modes
4. Сравнение различных режимов лазерного излучения
Рассмотрим режимы с различной длительностью и количеством импульсов в пакете, которые применяются в клинической практике при лечении патологии макулярной зоны, включая фовеа [17–22]. Проведем их сравнение на основе эффективно-селективного анализа (рис. 5). Как видно, режимы единичного импульса обладают наибольшими значениями эффективности и селективности одновременно. Увеличение количества импульсов приводит к снижению селективности. Однако, как было показано выше, режим 5 импульсов, 50 мкс, 2,4 % попадает в селективно-эффективное окно. Режим 95 импульсов, 50 мкс, 5 %, так же как и режим непрерывного излучения, обладает низкой селективностью, то есть приводит к повреждению нейросенсорной сетчатки и хориоидеи.
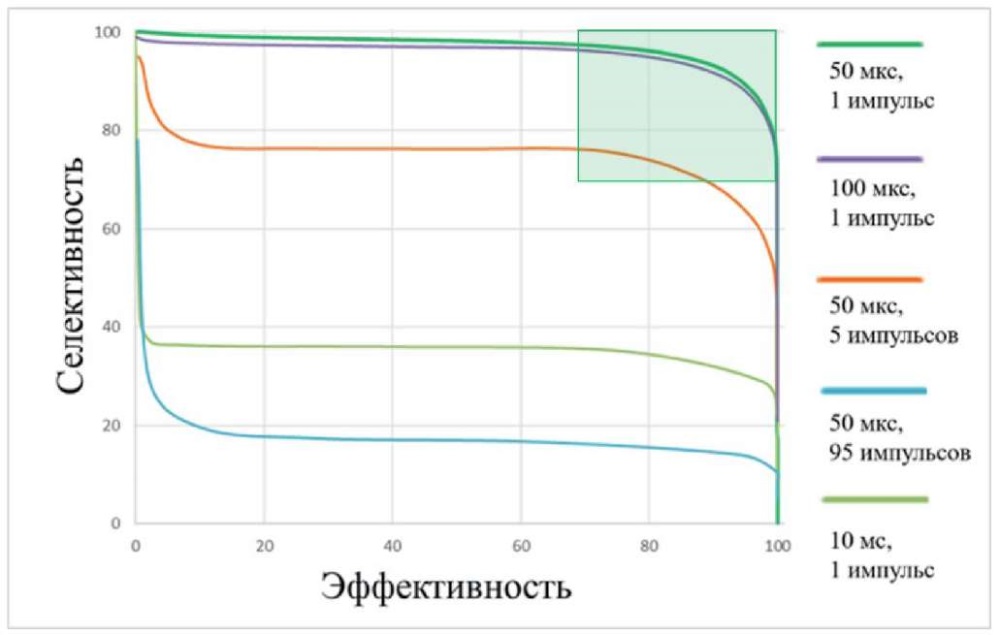
Рис. 5. Зависимость селективности от эффективности
для различных режимов лазерного излучения
Fig. 5. Dependence of selectivity on the efficiency
for different modes of laser light
Результаты моделирования различных режимов лазерного излучения приведены в таблице. Степень повреждения прилежащих к РПЭ структур отражает показатель относительной вредности, который является наименьшим у режимов единичного импульса и 2–5 импульсов в пакете. При данных режимах достигается высокая эффективность воздействия при очень низкой относительной вредности, что позволяет достичь клинического результата практически без повреждения нейросенсорной сетчатки и хориоидеи. Поэтому режимы с относительной вредностью меньше 1 предпочтительно применять при для лечения по технологии СМИРТ.
Таблица
Сравнение различных режимов лазерного излучения
по значениям селективности, эффективности
и относительной вредности
Table
Comparison of different modes of laser irradiation
by selectivity, efficiency and relative harmfulness
№ No | Режимы лазерного излучения (100 мкм, 577 нм) Laser radiation modes (100 microns, 577 nm) | Эффективность (η) Efficiency (η) | Селективность (ζ) Selectivity (ζ) | Относительная вредность (υ) Relative harmfulness (υ) |
1 | 80 мкс, 1 импульс, 2,0 Вт 80 microseconds, 1 pulse, 2.0 W | 90 | 91 | 0,09 |
2 | 110 мкс, 1 импульс, 1,5 Вт 110 microseconds, 1 pulse, 1.5 W | 90 | 90 | 0,10 |
3 | 50 мкс, 0,5 %, 40 мс, 4 импульса, 2,0 Вт 50 microseconds, 0,5 %, 40 ms, 4 pulses, 2.0 W | 80 | 73 | 0,30 |
4 | 50 мкс, 2,4 %, 10 мс, 5 импульсов, 1.5 Вт 50 microseconds, 2.4 %, 10 ms, 5 pulses, 1.5 W | 80 | 71 | 0,33 |
5 | 100 мкс, 4,9 %, 10 мс, 5 импульсов, 0,8 Вт 100 microseconds, 4,9 %, 10 ms, 5 pulses, 0.8 W | 80 | 67 | 0,39 |
6 | 10 мс, 50 мВт 10 ms, 50 mW | 80 | 33 | 1,62 |
7 | 20 мс, 15 %, 300 мВт 20 ms, 15 %, 300 mW | 99,9 | 17 | 5,96 |
8 | 50 мкс, 5 %, 0,1 с, 100 импульсов, 300 мВт 50 microseconds, 5 %, 0.1 s, 100 pulses, 300 mW | 99,9 | 7 | 13,36 |
9 | 50 мс, 50 мВт 50 ms, 50 mW | 99,9 | 6 | 15,51 |
10 | 200 мс, 5 %, 500 мВт 200 ms, 5 %, 500 mW | 99,9 | 4 | 25,05 |
Микроимпульсный режим (50 мкс, 5 %, 0,1 с) не является селективным, а по показателю относительной вредности даже уступает режиму с длительностью импульса 10 мс и сходен с режимом длительностью 50 мс. При данных параметрах происходит значительный рост температуры, приводящий к денатурации белков в прилежащих к РПЭ тканях. Следовательно, микроимпульсные режимы с более длительным импульсом, рабочим циклом и большим количеством импульсов в пакете приведут к большему повреждению сетчатки и хориоидеи.
На основе компьютерного моделирования установлено, что для технологии СМИРТ могут применяться микроимпульсные режимы с длительностью импульса не более 200 мкс, коротким рабочим циклом не более 5,0 % и количеством импульсов в пакете не более 5, с аккуратным подбором мощности с учетом персональных свойств пациента. Таким образом, избирательное воздействие лазерного излучения на РПЭ возможно при короткой длительности микроимпульса, небольшом количестве импульсов в пакете и большом расстоянии между импульсами, то есть при коротком рабочем цикле. Для соблюдения условий селективности необходимо учитывать персональные свойства.
5. Влияние индивидуальных свойств
В компьютерной модели учитываются две характеристики, зависящие от индивидуальных особенностей человека, такие как коэффициенты пропускания и поглощения лазерного излучения. Как известно, эти показатели уникальны у каждого человека и зависят от прозрачности оптических сред и концентрации меланина в РПЭ [17][18]. Поэтому их изменение будет влиять на значения эффективности и селективности. На рисунке 6 показано влияние коэффициентов пропускания и поглощения на результаты моделирования одиночного импульса длительностью 50 мкс.
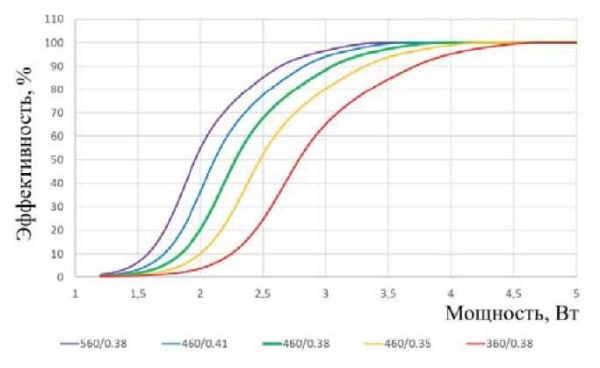
Рис. 6. Зависимость эффективности от мощности
при различных коэффициентах пропускания и поглощения
Fig. 6. Dependence of the efficiency on power
at different transmission and absorption coefficients
Видно, что изменения коэффициентов прохождения и поглощения приводят к изменению пороговой мощности на ± 0,5 Вт для уровня 50 % эффективности или изменению эффективности в диапазоне от 45 % до 95 % для значения мощности 2,75 Вт. То есть, одно и то же значение мощности лазерного режима может приводить как к недостаточному уровню воздействия, так и к избыточному.
Поэтому важно учитывать индивидуальные особенности пациентов при применении селективных режимов для технологии СМИРТ.
6. Рекомендуемые требования к техническим характеристикам лазерных установок для реализации селективного лечения
Настоящая работа позволяет предсказать режимы, при которых реализуется эффективное и селективное воздействие, при условии, что повреждение тканей происходит за счет термоденатурации протеинов. Важно отметить, что моделирование имеет ограничения и не может применяться при длительности импульса менее 20 мкс. При таких условия основным механизмом клеточного разрушения тканей становится термомеханический [8][9].
Современные лазерные установки имеют ограничения в технических характеристиках и мощности лазерного излучения. Компьютерное моделирование показало, что наибольшей селективностью обладает режим единичного импульса с высокой мощностью. Однако в клинической практике при лечении пациентов уровня мощности, которую можно установить на серийных лазерах, недостаточно. Поэтому для достижения высокой эффективности требуется увеличение длительности микроимпульса или количества импульсов в пакете, что приводит к снижению селективности и требует строгого учета персональных свойств.
Для реализации более селективного лечения наилучшими свойствами будет обладать режим единичного импульса длительностью от 25 мкс, что потребует увеличения мощности приблизительно до 6–8 Вт. Для большей вариабельности и комбинации параметров требуется возможность свободного изменения количества импульсов с шагом 1 импульс, длительности микроимпульса с шагом 5 мкс, мощности с шагом 100 мВт с возможностью продолжительного интервала между импульсами и короткого рабочего цикла.
Подобные режимы будут обладать высокой эффективностью и селективностью (90–99) одновременно. Реализация режимов с более короткой длительность импульса и высокой мощностью позволит достичь такого уровня селективно-эффективного размена, что ошибки, связанные с учетом персональных свойств, не приведут к существенному снижению селективности.
Учитывая, что при работе с селективными режимами требуется высокая мощность, важно, чтобы в лазерных установках срабатывала блокировка подачи импульса при превышении совокупной энергии, например при случайном выборе длительного времени воздействия.
7. Критерии безопасного применения селективных микроимпульсных режимов при лечении макулярной зоны, включая фовеолу
Г. И. Желтов посвятил много лет изучению условий безопасности при работе с лазерным излучением и указывал, что правила и нормы должны быть пересмотрены. Многие отдаленные последствия применения лазерного излучения еще не изучены, поэтому при лечении доза облучения должна быть сведена к предельному минимуму. Современные офтальмологические лазерные установки, оснащенные микроимпульсным режимом, относятся к 4-му классу опасности и требуют особо внимательного подхода и грамотной технологии эксплуатации. При создании нормативных документов по безопасности работы с лазерным излучением и классов опасности лазерного излучения предельно допустимые уровни (ПДУ) лазерного воздействия определяли исходя из выявления офтальмоскопически видимого порога лазерного коагулята с вероятностью 50 %. Офтальмоскопический порог является грубым и определяется при необратимом разрушении нейросенсорной сетчатки [1].
Селективное воздействие не визуализируется офтальмоскопически, а регистрируется по данным коротковолновой АФ (488 нм). Лечение по технологии СМИРТ проводится в центральной зоне сетчатки, включая фовеолу, отвечающую за максимальные зрительные функции. Следовательно, подходы к определению ПДУ по офтальмоскопическому порогу не подходят для оценки безопасности применения селективных режимов. Для определения ПДУ необходимо использовать более чувствительный порог по данным АФ с корректной обработкой данных и оценкой опасности воздействия по степени повреждения прилежащих к РПЭ структур. Показатель относительной вредности (υ) – более корректный критерий, так как количественно описывает степень повреждения нейросенсорной сетчатки и хориоидеи и является лучшим параметром для оценки степени безопасности лазерного воздействия.
ЗАКЛЮЧЕНИЕ
Определено качество микроимпульсного режима лазерного излучения при эффективности, равной 90 %. При селективности менее 50 % режим является неселективным, а при селективности более 67 % – селективным. Проведено сравнение различных режимов лазерного излучения и предложены параметры для технологии селективной микроимпульсной индивидуальной ретинальной терапии на существующих серийных офтальмологических лазерных установках. Усовершенствован подход к определению условий безопасности при лечении заболеваний макулярной зоны селективными микроимпульсными режимами высокой мощности с учетом сохранности нейросенсорной сетчатки и хориоидеи по показателю относительной вредности, который не должен превышать 1. Предложены параметры и режимы для будущих лазерных установок с высокими значениями (более 90–99) эффективности и селективности одновременно, которые могут быть реализованы производителями и внедрены в клиническую практику. Таким образом, для селективной микроимпульсной индивидуальной ретинальной терапии макулярной зоны на существующих лазерах могут применяться микроимпульсные режимы с длительностью импульса не более 200 мкс, коротким рабочим циклом менее 5 % и количеством импульсов в пакете не более 5, относительной вредностью менее единицы, с подбором мощности излучения, учитывающей персональные особенности пациента.
Список литературы
1. Желтов Г.И. Вопросы лазерной офтальмологии. Проблема безопасности при работе с лазерами. М.: Апрель. 2013: 15–31.
2. Ivanova E.V., Volodin P.L. Development of the selective micropulse individual retinal therapy depends on age and type on the Fitzpatrick scale. Graefes Arch Clin Exp Ophthalmol. 2023; 261 (2): 381–390. DOI: 10.1007/s00417-022-05800-9
3. Володин П.Л., Иванова Е.В., Соломин В.А. Возможности современных методов диагностики и компьютерной обработки данных с помощью программы «Фемтоскан» для выявления слабых термических повреждений клеток ретинального пигментного эпителия. Лазерная медицина. 2018; 22 (1): 52–56. URL: https://elibrary.ru/item.asp?id=35101048&ysclid=logu7k8yiq750038209
4. Framme C., Schüle G., Brinkmann R., Birngruber R., Roider J. Fundus Autofl uorescence After Selective RPE Laser Treatment. Ophthalmologe. 2002; 99 (11): 854–860. DOI: 10.1007/s00347-002-0684-z
5. Желтов Г.И. Биофизика деструктивного действия надпорогового лазерного излучения на ткани глазного дна. II Всероссийский семинар «МАКУЛА 2006». Материалы научно-практической конференции. Ростов-на-Дону. 2006: 71–85.
6. Иванова Е.В., Володин П.Л. Физическое моделирование для оценки воздействия микроимпульсных режимов лазерного излучения на хориоретинальный комплекс человеческого глаза на основе теории активированных комплексов. Лазерная медицина. 2022; 26 (3-4): 47–55. DOI: 10.37895/2071-8004-2022-26-3-4-47-55
7. Ivanova E.V., Volodin P.L, Guskov A.V. Determination of Micropulse Modes with Targeted Damage to the Retinal Pigment Epithelium Using Computer Modeling for the Development of Selective Individual Micropulse Retinal Therapy. Curr Eye Res. 2022; 47 (1): 107–114. DOI: 10.1080/02713683.2021.1962360
8. Alt C., Pitsillides C.M., Roegener J., Lin C.P. Monitoring intracellular cavitation during selective targeting the retinal pigment epithelium. Proc SPIE. 2003; 4951: 48–55. DOI: 10.1117/12.477956
9. Schuele G., Rumohr M., Huettmann G., Brinkmann R. RPE damage thresholds and mechanisms for laser exposure in the microsecond-to-millisecond time regimen. Invest Ophthalmol Vis Sci. 2005;46 (2): 714–719. DOI: 10.1167/iovs.04-0136
10. Lavinsky D., Wang J., Huie P., Dalal R., Lee S.J., Lee D.Y., Palanker D. Nondamaging Retinal Laser Therapy: Rationale and Applications to the Macula. Invest Ophthalmol Vis Sci. 2016; 57 (6): 2488–2500. DOI: 10.1167/iovs.15-18981
11. Wang J., Quan Y., Dalal R., Palanker D. Comparison of continuous-wave and micropulse modulation in retinal laser therapy. Invest Ophthalmol Vis Sci. 2017; 58 (11); 4722–4732. DOI: 10.1167/iovs.17-21610
12. Schlott K., Koinzer S., Ptaszynski L., Bever M., Baade A., Roider J., Birngruber R., Brinkmann R. Automatic temperature controlled retinal photocoagulation. J Biomed Opt. 2012; 17 (6): 061223. DOI: 10.1117/1.JBO.17.6.061223
13. Sanchez-Ruiz J.M. Protein kinetic stability. Biophys Chem. 2010; 148 (1-3): 1–15. DOI: 10.1016/j.bpc.2010.02.004
14. Godoy-Ruiz R., Ariza F., Rodriguez-Larrea D., Perez-Jimenez R., Ibarra-Molero B., Sanchez-Ruiz J.M. Natural selection for kinetic stability is a likely origin of correlations between mutational effects on protein energetics and frequencies of amino acid occurrences in sequence alignments. J Mol Biol. 2006;362 (5): 966–978. DOI: 10.1016/j.jmb.2006.07.065
15. Гапеева Т.А., Глазков В.Н., Подольцев А.С., Желтов Г.И., Мешков Г.Г. Лазерный метод определения температурной зависимости константы скорости реакции фотокоагуляции in vivo. Весцi АН БССР. Серыя фiзiка-матэматычных навук. 1986; 3: 81–85.
16. Желтов Г.И. Воздействие интенсивного оптического излучения на ткани глаз: исследования и приложения. Автореф. дисс. докт. мед. наук. Минск. 1996. 15 с.
17. Geeraets W., Williams R., Chan G., Ham W., Guerry D., Schmidt F. The relative absorption of thermal energy in retina and choroid. Invest Ophthalmol Vis Sci. 1962; 1: 340–347.
18. Weale R.A. Age and the transmittance of the human crystalline lens. The Journal of Physiology. 1988; 395 (1):. 577–587. DOI: 10.1113/jphysiol.1988.sp016935
19. Ivanova E.V., Volodin P.L., Zheltov G.I. New technique of treatment acute central serous chorioretinopathy based on selective infl uence of short laser pulses on retinal pigment epithelium. European Journal of Ophthalmology. 2017; 27 (2): 67.
20. Volodin P.L., Ivanova E.V. Clinical evaluation of individualized and navigated microsecond pulsing laser for acute central serous chorioretinopathy. Ophthalmic Surgery Lasers and Imaging Retina. 2020; 51: 512–520. DOI: 10.3928/23258160-20200831-06
21. Zhou L., Lai K., Jin L., Huang C., Xu F., Gong Y., Li L., Zhu Z., Lu L., Jin C. Subthreshold Micropulse Laser vs. Conventional Laser for Central Serous Chorioretinopathy: A Randomized Controlled Clinical Trial. Front Med (Lausanne). 2021. DOI: 10.3389/fmed.2021.682264
22. Kim J.Y., Park H.S., Kim S.Y. Short-term efficacy of subthreshold micropulse yellow laser (577 nm) photocoagulation for chronic central serous chorioretinopathy. Graefes Arch Clin Exp Ophthalmol. 2015; 253 (12): 2129–2135. DOI: 10.1007/s00417-015-2965-7
Об авторах
Е. В. ИвановаРоссия
Елена Владимировна Иванова, кандидат медицинских наук, врач-офтальмолог
отделение лазерной хирургии сетчатки
Москва
П. Л. Володин
Россия
Павел Львович Володин, доктор медицинских наук, заведующий отделом
отдел лазерной хирургии сетчатки
Москва
Рецензия
Для цитирования:
Иванова Е.В., Володин П.Л. Определение режимов безопасного применения селективной микроимпульсной индивидуальной ретинальной терапии макулярной зоны с помощью моделирования на основе теории активированного комплекса. Лазерная медицина. 2023;27(2):22-31. https://doi.org/10.37895/2071-8004-2023-27-2-22-31
For citation:
Ivanova E.V., Volodin P.L. Determination of modes for safe application of selective micro-pulse individual retinal therapy of the macular zone using the modeling based on the theory of activated complex. Laser Medicine. 2023;27(2):22-31. (In Russ.) https://doi.org/10.37895/2071-8004-2023-27-2-22-31
JATS XML


























